| |
���� |
�Ǐ� |
�����j�E�����o�H |
�����@�E�\�h�E���� |
���̑� |
| �������� |
�ԗ��A���[�oEntamoeba histiolytica |
�E���A���[�o�ǁF��ᇁA䕃[���[��S���ցB
�E���NJO�A���[�o�ǁF�̔^ᇂ̕p�x�������B
�E���Ǐ�F�X�q�ۗL�ҁB��x�����ǂ��Ȃ��A�܂��͉��Ă��疳�Ǐ�ɂȂ�B�O�҂�ڐG�ے��ҁA��҂����ے��҂Ƃ����B�X�q����o��������B |
�h��F�q�g���傾�����ɃC�k�A�l�R�A�T���ȂǁB
�h�{�^���咰�ɂđ��B�B���ւƂƂ��ɉ��~���ĔX�q�^�ɂȂ�A�X�q�^�̌o���ێ�ɂ�芴������B�h�{�^�͈��ݍ���ł��݉t�ŎE�����̂Ŋ������Ȃ��B
|
�����F���N�W�{���璎�̂����o�B�̔^ᇂł͂w���A�b�s�A�����g�ȂǁB
�Ɖu�w�I�f�f�@�F�Ԑڌu���R�̖@�i�h�e�`�j�A�y�f�R�̖@�i�d�k�h�r�`�@�j�ȂǁB
�\�h�F���ݐ�����̔X�q�̌o���ڎ��\�h�B
���ÁF���g���j�_�]�[���B�R���ܕ��p
|
��a�����̑咰�A���[�o�͐Ԍ����̕ߐH�������Ȃ����ԗ��A���[�o�ł͌�����B�܂��A�J���I�\�[�����j�̒��S�ɂ���B
���z�F���E�� |
�a�������R�����A���[�o
�P�D�l�O�����A�t�H����Naegleria fowleri
�Q�D�A�J���g�A���[�o�J���o�[�g�\�jAcanthamoeba culbertsoni |
�P�D�������A���[�o�������]���i�o�`�l�j�F�R�`�S���Śq�f��ӎ���Q�A�T�`�U���Ŏ��S�B
�Q�D�A���[�o�������]���i�`�l�d�j�F���̓��a�������ƍl�����Ă���A�o�߂͂o�`�l���ɏ��Ŕ]�a���̖������ǂ�A���[�o���]�����������B�܂��R���^�N�g�����Y�g�p�҂̃A���[�o���p�����i��ᇁj��������B
|
�P�D���j�␅���ŕ@�S������k�_�o����Ĕ]���ɐN���B
�����j�F�O�͂̏����ɂ��h�{�^�A�ږь^�A�X�q�^������ɂ��ڍs������B
�Q�D�畆�A�x�A��A���B��A���ٌ����Ȃǂ̏����a�����猌�s���ɔ]�ɓ]�ځB |
�P�D�����F�]�Ґ��t����̌��o�B
���ÁF��ʂɍ���������̃A���z�e���V���a�̐Ò��A�e�g���T�C�N�����A�T���t�@�܂̓��^�B
�Q�D�����E���ÂƂ��P�̂o�`�l�Ɠ��l�ł��邪��͂�����I�Ȏ��Ö@�͂Ȃ��B |
�P�D���z�F���E���a���͑�]�玿�Ɍ��ǂ��A�A���[�o�̑S�g�����͌����Ȃ��B
�Q�D���z�F���E��
|
| �E�q���� |
�}�����A����Plasmodium�`
�P�D�O���M�}�����A�����@P.vivax
�Q�D�M�єM�}�����A�����@P.falciparum
�R�D�l���M�}�����A�����@P.malariae
�S�D���`�}�����A�����@P.ovale
|
�����]�C�g���o���̐Ԍ����j��ɂ��A�n�����n���A��_�f�ǁA�őf�������̑̉������h���ɂ��M����
�}���}�����A�F�M����A�n���A�B����咥�Ƃ���B�M����͈����������M�̎ܔM���������������M���̎����B���̎����͎O���A���^�͂S�W���A�l���͂V�Q���B
�����}�����A�F�M�єM�}�����A�ɂ��B�����Ȃ̂͑S����̐Ԍ����ɐN�����邽�߁i�O���A���^�͗c��A�l���͘V��Ԍ����ɐN���j36�`48�����ƁB������ɏd�č����ǁi�t��Q�j�ADIC�A�o���A�V���b�N�A���F�f�A��r�o���鍕���M�ȂǁB
�����}�����A�F�M�^�͕s��ƂȂ邪�A�n�����B������B
�Ĕ��F
�ĔR�����Õs���Ō����c���̐ԓ��^�������B�ɂ��B
�Ĕ����O���M�A���^�M�ɂāA�̍זE���̃q�v�m�]�C�h�ɂ��B
�������F�O���A���^:2�T�@�l��:30���@�M��:12�� |
�����o�H�F�X�|���]�C�h���������n�}�_���J�̎h���B���ɗA���≘�����ːj�ȂǁB
���z�F�O���M�͔M�т��牷�т܂ōL�����z�B�l���M�A�M�єM�́A�M�сA���M�тɕ��z�B���^�́A�M���уA�t���J�̈ꕔ�Ɍ��ǁB
�����j�F�i�G�b�Z���V�������a�wp62�j
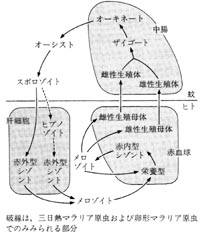
|
�����F�������̌��w����є��w�h���W�{���M���U���F���ċ����B
�O���M�FSchufner���_�B
�M�єM�F�֏�̂̂݁BMaurer���_�B���`�FSchufner���_
�}�����M����Ö@�F
�@�N�����L���A�t�@���V�_�[�����B���_�L�j�[�l�@�A�ƇB�͔D�w�ɂ͋֊��B
��ܑϐ��}�����A�̔M����Ö@�F
�N�����L���ϐ��̓x�����ɂ��A�A�B�A�R�������i�e�g���T�C�N�����Ȃǁj�p����B
�d�ǃ}�����A�ً̋}�Ö@�F���_�L�j�[�l
�Ĕ��h�~�F�v���}�L���i�O���M�Ɨ��^�ɑ��čs���B�q�v�m�]�C�h�ɑ��āj
�\�h�F�n�}�_���J�̋쏜�B�R�}�����A��̗\�h�����B |
�X�|���]�C�g��������̋z�����ɑ��t�B���璍�������ƁA�ꎞ�Ԉȓ��Ɋ̍זE�ɐN�����Ĕ��炵�A�����̃����]�C�g����B�O���M�Ɨ��^�ł́A�ꕔ�̃X�|���]�C�g���Î~��Ԃő��B�i�q�v�m�]�C�g�j���Ĕ��̌����B
�����]�C�g�̐ԊO�^�͐Ԍ����ɐN�����A�֏�́A�A���[�o�́A�V�]���g�Ɣ��炵�ĐԌ�����j�āA�V���ȃ����]�C�g�����i�M�єM�}�����A�ł͗֏�̈ȍ~�̔��炪�]�A�́A�B�A�t�Ȃǂ̖э��ǂɂčs����̂ŁA�������ł͌����Ȃ��j�ԓ��^�́A���Y�̐��B��̂�����Ď��ŁB�z�����ɔ}���Ɏ�荞�܂ꂽ���B��͈̂ݓ��Ō��������B�̂ɂȂ�B���ꂪ�Z�����ăU�C�S�[�g�ɂȂ�A���ʼn^�����̂���I�[�L�l�[�g�ɂȂ�B�����āA�ݕǂ���ʂ��ĖE�X�́i�I�[�V�X�g�j�ɂȂ�X�|���]�C�g���`������B�X�|���]�C�g�������`�������ƖE�X�̂̔j��ɂ���đ̍o�ɕ��o����A���t�B�ɏW�ς��Ċ������ƂȂ�B
|
| �g�L�\�v���Y�}Toxoplasma gondii |
��V���g�L�\�v���Y�}�ǁF�S�咥��i�P�j�Ԗ��������A�i�Q�j�����ǁA�i�R�j�]���ΊD�����A�i�S�j���_�E�^����Q�A���ɔ��M�A���t�A�����p�ߎ�A�n���A�]���A�S�؉��ȂǁB
��V���g�L�\�v���Y�}�ǁF�ʏ�قƂ�Ǖs���������i���܂Ƀ����p�ߎ�j�����Ɖu�\���ቺ����ƌ��������S�g���ɑ��B�A�a�����`���������p�߉��A���M�ȂǁB�ŋ߂`�h�c�r���҂̃g�L�\�v���Y�}�]���̕��������ڂ���Ă���B
|
�h��F�l�R���I�h��B�q�g���͂��ߑ����̚M���ނⒹ�ނ����ԏh��B
�����o�H�F
�P�D�u�^��r�̓��̐��H�ɂ��X�q����уI�[�V�X�g�̊����B
�Q�D�l�R�̕��֒��̃I�[�V�X�g�B
�R�D�l�R�Ƃ̐ڐG�����B
�S�D������̂���َ��ւ̃^�L�]�C�g�ɂ��ٔՂ�ʂ������������B |
�����F�����̌��o�͍���Ȃ��߁A
�����w�I�f�f�F
�E�F�f�����iSabin -Feldman's dye test�j
�EIHA:�Ԍ����ÏW����
�ELA:���e�b�N�X�ÏW����
���ÁF�s�����T�~����A�Z�`���X�s���}�C�V���ƁA�T���t�@�܂̕��p�B
�\�h�F�l�R�̕��ւɒ��ӁB��r�Ȃǂ̐��H��������B�������ɂ����ӁB |
���z�F���E��
���ԏh����ł́A�ێ悳�ꂽ�X�q�܂��̓I�[�V�X�g�͏����ŒE�X���A�h�{�^��X�|���]�C�g�ɂȂ�A���s���Ɋe���ɉ^��זE���ŕ������B�i���̔�����̌������^�L�]�C�h�j�B�h��̍R�̎Y���ɂ�A�X�q�^�ɂȂ�B
�I�h����ł͔X�q�܂��̓I�[�V�X�g�͏����ŒE�X���A�����̃����]�C�g����o�A���̈ꕔ�����Y�̐��B��̂ƂȂ�A���B�̂ɔ��炷��ƗL�����B���s���ėZ���̂��`���A���ꂪ�I�[�V�X�g�ɂȂ�A���ւƂƂ��ɔr�o�B
|
| ���ޕs�\ |
�j���[���V�X�`�X�J���j�@Pneumocystis carinii |
���̓��a�������B���ċz�A���M�A�����Ōċz����ƃ`�A�m�[�[��悷��x���B�d�v�ȏ����Ƃ��Ĕx�E�эǃu���b�N�ɂ��Pao2�̂P/2�`1/3�ɒቺ�B |
�����o�H�F�m�肳��Ă��Ȃ����A�X�q�̌o�C�������ƍl�����Ă���B |
�����F�\ႂ���ޗ�����̒��̂̌��o�Őf�f�B
���ÁF
�@�C�Z�`�I���_�y���^�~�W���i�{���̓A�t���J�����a�̎��Ö�j
�AST�i��̧�ķ�ްقƁA�������сj |
�Ɖu�ቺ�Ŕ��ǁBAIDS�┒���a�Ȃǂ̂Ƃ��Ɋ�������������a�������B |
| �ږђ��� |
�����u���ږђ�
Giardia lamblia |
������ږђ���
�����ł͖��Ǐ�B�����㕔�̍L�Ăȉ��ǂƋz����Q���Ď��b�������B�_���ւ̊Œ_�`�T�ɂ��_�X��
|
�����o�H�F�X�q�̌o�������ŁA�������H���̐ێ�ɂ��B
�h�{�^�F�����𒆐S�ɍ��E�Ώ́B4�̕ږ�
�X�q�^�F2�`4�̊j�I
�h��F�q�g |
�����F�L�`�ւ���X�q�A�����ւ���h�{�^��X�q�����o�B
���ÁF���g���j�_�]�[���A�`�j�_�]�[���i��������D�w�A���t�����A�펿�I���_�a�ɂ͋֊��j�B�L�i�N�����B
|
���z�F���E���ɍL�����z�B�Ƃ��ɔM�сE���M�тɑ����B |
�S�g���R���i�X
Trichomonas vaginalis |
��A�E���B��ږђ���
�S������́B���o�Ǐ�������Ȃ����ҁi��ɒj���j������A�������ɂȂ肤��B |
�h�{�^�̂݁B�������S�Ƃ��̕t�����B�Ɋ���B
�����o�H�F�����Ȃǂ̐ڐG�����B����ł��������蓾��B |
�����F�V�N���S���啨�܂��͔A�����啨������
���ÁF���g���j�_�]�[���A�`�j�_�]�[���i�D�w�ɂ͋֊��j�B�j���Ԃ̑��݊����i�s���|�������j�����邽�ߔz��҂��������ÁB |
���z�F���E��
�\�h�F���a�\�h�ɏ�����B |
�K���r�A�g���p�m�\�[�}
Trypanosoma brucei gambiense
���[�f�V�A�g���p�m�\�[�}�ƂƂ��ɃA�t���J�����a�A�܂��̓K���r�A�g���p�m�\�[�}�ǂ̕a���́B |
�ȉ��A���t�E�g�D�ږђ���
�����F���M�A���M���������A���ɁA�q�f�A�w�ɁB
�����F���B��A�����p�߂Ƃ��ɍ��������p�ߎ�傪�������E�B���^�[�{�g������
�����F�����_�o�Ǐ����ƂȂ�A���s�Ȃǂ̏�Q���獨���Ɋׂ�A�����͍����ǂ����Ď��S�B���̊Ԃ͂Q�`�R�N�B�����ǂ͂Q�`�R�������납�猩����B |
�����j�F�������̃g���|�}�X�`�S�[�g�^���c�F�c�F�o�G�ɋz�������ƁA�����ŕ������B�A���t�B�ŃG�s�}�X�`�S�[�g�^���犴���^�̃g���|�}�X�`�S�[�g�^�ɔ��炷��B�z�����ɂ�����q�g�ɒ�������B
�����o�H�F�����c�F�c�F�o�G�̎h���B
�h��F�q�g�݂̂����R�h��B |
�����F���t�A�����p�ߐ��h�t�A�]�Ґ��t���猴�����o�B�h���l�̒����ɂ킽�钘���B�d���h�r�`�ȂǁB
���ÁF�X���~���A�y���^�~�W���B�]�ǂ��ꍇ�g���p���T�~�h�A�������\�v���[���B�������y���^�~�W�������������������B
�\�h�F�c�F�c�F�o�G�̎h������B
|
���z�F�ܓx����k�P�T�x�̃A�t���J�������B
���[�f�V�A�g���p�m�\�[�}�̕��������ŋ}���B
|
| �N���[�Y�g���p�m�\�[�}�@Trypanosoma cruzi |
�V���[�K�X�a�A�A�����J�g���p�m�\�[�}�ǁB
�}�����F�����͏����B�h�����ɔ��Ԃ���ᎁi�V���S�[�}chagoma�j����B���ō��M���A�S�g�ɕ�����݂�B�Б����̊��َ��͂̕���i���}�[�j���nj�j�͍ł������I�ȏ����Ǐ�ł���B
�������F�N�P����̕a�ςf����Ǐ\�N�]�ɂ킽���Ċɏ��ɐi�s����B�悭������̂͐S�؉��A���������S�s�S�A���S�ƌĂ��S�����A�����ǔ��i����H��
megaesophagus�A���匋�� megacolon�j�ł��邪�A�_�o�^������B���l�̏ꍇ�͍ŏ����疝���a�^�����ǂ�Ⴊ�����B |
�����j�F�T�V�K���ނ̏����ǂŃg���}�X�`�S�[�g�^�ɂĔ���B�����ŃG�s�}�X�`�S�[�g�^�ƂȂ��ĕ������B�B�㒰�Ńg���|�}�X�`�S�[�g�^�ɂȂ��ĕ��֒��ցB���ꂪ�畆���ʂ�S������̐N���A��ԓ��n�זE���ɂăA�}�X�`�S�[�g�^�ɂȂ��čזE��j�A�ĂэזE���ɐN�����J��ւ����B
�����o�H�F�T�V�K���̕��֒��ɔr�o����銴���^���̂̔畆���ʂ�S������̐N���B
�I�h��F�q�g�A�T���A�A���}�W���A�C�k�A�l�R�ȂǁB |
�����F�������A�����p���h�t�̃M���U���F�B�W�{���ɒ��̌��t�A�����ޗ��̃������b�g�ێ��NNN�|�n�Ŕ|�{���A�G�s�}�X�`�S�[�g�^�̌��o�B�������T�V�K���Ɋ��҂���܂���O���f�f�@�B
���ÁF������͂Ȃ��B���s�n�ł�nifurtimox�i�����������j
�\�h�F�T�V�K���̖h���Ƃ��̎h���̉���B
|
���z�F�����
�h�����ӎ��ɑ~���āA���̂����荞�ނ��Ƃ������B���s�n�ł́A�A�������A�ٔՊ���������B
|
| �h�m�o�����[�V���}�j�A�Q�@Leishmania donovani complex |
�J���A�U�[���i���M�a���畆�����A�F�f�����j�A�_���_���M�Ȃǂ̓������[�V���}�j�A�ǂƂ��Ēm����B
��ȏǏ�͔��M�A�s�����A�H�~�s�U�ŔM�ѐ����B�ǂƌĂ�钘�����B��A�̎�����A�����O���u�������ǂ��B������P�`�T�N���o�ăJ���A�U�[�����畆�^�i�o�j�c�k�j���邱�Ƃ�����B
|
�����j�F�T�V�`���E�o�G�̒������Ńv���}�X�`�S�[�g�^�ő��B���A���Ɉڍs���ăA�}�X�`�S�[�g�^�i2�`4��m�̗��~�n�j�ɂċz�����ɏh��ɒ����B�l�̓��ł͖ԓ��n�זE��A�H�זE���ɃA�}�X�`�S�[�g�^�̊Ƒ��B�B
�����o�H�F�T�V�`���E�o�G�̋z���ɂ��v���}�X�`�S�[�g�̒����B�܂�ɃA�}�X�`�S�[�g�ɂ��o�ٔՊ���������B
|
�����F�����ޗ����M���U�܂��̓��C�g���F���A�A�}�X�`�S�[�g�̏ؖ��B�܂����t���V�|�n�ɐڎ킵�v���}�X�`�S�[�g���ؖ��B
�Ɖu�f�f�F�x���^��Montenrgro�@�A�o�b�q�ȂǁB
���ÁF�y���g�X�^����O���J���^�C��
�\�h�F�T�V�`���E�o�G�̋z���������B
|
���z�F�C���h���嗤�A�������k���A���\�A�암�A���ߓ��A�n���C���݁A����ĂȂǁB
���ߓ��⋌�\�A�암�ł�leishmanization�Ƃ������̐����N�`�����Â�������{����Ă���B
|
|
�P�D�M�у��[�V���}�j�A��Q
�Q�D���L�V�R���[�V���}�j�A��Q�ȂǁB
|
���嗤�A�V�嗤�̔畆���[�V���}�j�A��
���ɐ��̒�ᇁi�Ό���j�B�畆���[�V���}�j�A�̕ʖ��i�`�N������ᇁj�̓S�����œ����J���҂ɊO���̒�ᇂ����������邱�Ƃ���g����悤�ɂȂ������t�ł���i�`�N���Ƃ̓S���̖̂��Ɓj�B |
�O�q�̃h�m�o�����[�V���}�j�A�Q�Ɠ����B |
�O�q�̃h�m�o�����[�V���}�j�A�Q�Ɠ����B |
���[�V���}�j�A�ǂɂ�
�P�D�������[�V���}�j�A��
�Q�D�畆���[�V���}�j�A��
�R�D�S���畆���[�V���}�j�A��
�S�D�Ĕ����畆���[�V���}�j�A�ǂ�����B |
| �@�ђ��� |
�咰�o�����`�W�E��
Balantidium coli |
���Ǐ�̂��̂���y�x�̐��l�������A���邢�͕��ɁA�q�f�A�̏d�����ɔS���ւ�悷����̂܂ő��l�ł���B |
�����j�F�h��Ɍo���ێ悳�ꂽ�X�q�͏����ŒE�X���A�h�{�^�͑咰�ɒB����Ɛ��n���ĉ���ő��B���邪�ڍ����c�ށB
�����o�H�F�X�q�̌o�������ł��邪�A�������Ă����Ǐ�ɑω߂���u�^�Ƃ̐ڐG�ɂ����̂��ŏd�v�ł���B
|
�����F�����ւ���h�{�^���́A�L�`�ւ���X�q�����o�B
���ÁF���g���j�_�]�[����e�g���T�C�N�������^���L��
|
�@�ђ��ނ͑̕\�͑@�тɕ����A�̑O�[�̍זE���A��j�Ə��j�̂Q�j��L���A���B�͂Q����ƗL�����B�̐ڍ����s���̂������B���R�E�ɂ͑�����ނ������邪�l�̊�͂P�B���E�ɍL�����z���A�e�n�̃u�^�ɍ����Ɋ������Ă��� |
| �@ |
���� |
�Ǐ� |
�����j�E�����o�H |
�����@�E�\�h�E���� |
���̑� |
| �[�t�� |
�L�ߗ����𒎁i�k�����Y�j�@
Diphyllobothrium latum
�i���{�Y�̂��͓̂��{�C�����𒎁@Diphyllobothrium nihonkaiense�j
|
���������玩�R���̔r���A�����A���ɂȂǁB
�𒎕n���i�𒎂̃r�^�~��B12�̒D��ɂ�鈫���n���j |
�����j�F�����i��������R���V�W�E���j����ꒆ�ԏh��F�P���~�W���R�i�v���Z���R�C�h�j����ԏh��F�T�N���}�X��T�P�i�v�����Z���R�C�h�j���I�h��F�q�g�A�C�k�A�l�R�A�F�Ȃǁi���{�C�����𒎂̓q�g�j�B
�����o�H�F��ԏh��ł���T�P��}�X�̐��H�B |
�����F�������ɂ�钎���̌��o�B�r�����ꂽ�А߂̑g�D�w�I�����B
���ÁF�v���W�J���e���A�A�~�m�T�C�W���B�K�X�g���O���t�B���@�ADamaso de Rivas�@�B
�\�h�F�T�N���}�X��T�P�̎h�g�₷���ɒ��ӁB |
���z�F�t�B�������h�̌Β��S�B�܂��͓��{�B
���Ǔ��ɊB |
�}���\��������
Spirometra erinacei |
�}���\���ǒ��ǁF�c���ڍs�ǂ̈�B�v�����Z���R�C�h���g�D���Ɋ��A�V�������ǐ��畆��ᎁi����ɍזE�Z���⌋���g�D�����j��������B�D�_�������A�h���d���x���̏㏸�B�������܂ꂾ����͂���B |
�����i��������R���V�W�E���j����ꒆ�ԏh��F�P���~�W���R�i�v���Z���R�C�h�j����ԏh��F�����ށi�J�G���j�A��ށi�ցj�A���ށA�M���ނȂǁB�i�v�����Z���R�C�h�j�B�q�g�i�ҋ@�h��j�ł͗c���ڍs�ǁ��I�h��F�C�k�A�l�R�A�L�c�l�A�g���Ȃ� |
�����F�����I�畆�؊J�AOuchterlony�@�A�Ɖu�d�C�j���@�Ȃnj����Ɖu�w�I�����B
���ÁF�O�ȓI�E�o�A�v���W�J���e���B
�\�h�F�J�G���A�w�r�A�j���g���Ȃǂ̐��H�������B�~�W���R�̂������ȉ����̐ێ�������B |
�ǒ��ǁF�����𒎂̗c���i�v�����Z���R�C�h�j���l�̂ɊA���̐������s���ł���i�ǎ��j�Ƃ����Ӗ��Ōǒ��ǂƌĂꂽ�B
���ɉ�B�ǒ��ɂ���B�ǒ��ǂ�����B�}���\���ǒ��ƈقȂ�̓��ŕ������B���邽�ߓ����ɂ��N�P���A���Â͍���Œv���I�ł���B
�v�����Z���R�C�h��f�ʂɂ��ĕW�{�Ƃ��Ă݂�ƐΊD���̂�������B |
�啡�B���
Diplogonoporus grandis |
�����㕔�Ɋ��A���ɁA�����A�H�~�s�U�A�S�g���ӊ��A���S�E�q�f�ȂǏ�����Ǐ���������B |
�����j�F�悭�킩���Ă��Ȃ��B�N�W�����璎���r������ꒆ�ԏh��F�P���~�W���R�i�����I��1��ފm�F���ꂽ�̂݁j����ԏh��F�C���V�A�A�W�A�T�o�Ȃǂ̏��`�Q�W���Ƌ^���Ă���B |
�����F���֒��̒������o�B���R�r�����ꂽ���̓��߂�А߂̌`�ԁA�g�D�w�I�����B
���ÁF�L�ߗ����𒎂Ɠ����B
�\�h�F�������s���̂��߁A���݂͓K���ȗ\�h�@���Ȃ��B |
���z�F���{���L�ƌ�����B |
| �~�t�� |
�����
Taeniarhynchus saginatus |
����𒎏ǁF�S���̌y���ǁB���ʂ͎��o���Ȃ��B���ɕ��ɂƑ̏d�����ւɍ������Ĕr�o����ċC�t�����Ƃ������B |
�����j�F���͕А߂ƂƂ��ɕւɍ������ĊO�E�֏o�āA���ȂǂƋ��ɃE�V�ɐێ悳��āA�����ɂĘZ��c�����V������B����^�זE���Ŗ���X�����ɂȂ�A�H���Ńq�g�֊����B�����ɂĔX�����͔X���̓��߂�|�]���Ē��ǔS���ɋz������B
���ԏh��F�E�V�@�I�h��F�q�g |
�����F�������ɂ�钎���z�����͏��Ȃ��B�Z���t�@�������͌����@�����݂���B
���ÁF�L�ߗ����𒎂Ɠ����B
�\�h�F�����̏[���ȉ��M�B |
���z�F���E��
�H�K���ɂ��C�X�������k�ɑ����B
�S�`�U���ɂ��Ȃ�A�O�E�ŕАߎ��g�������������B |
�L���
Taenia solium |
�����̏ꍇ�͖���𒎏ǂƓ����B
�L��X�����ǁF�c���ɂ��B�����_�o�A�牺�A��ȂǂɔX���`���B |
�����j�F���͕А߂ɓ������܂܊O�E�ɏo�āA�u�^�Ɍo���I�ɐێ悳���B�����ɂĘZ��c�����V�����A����ŗL��X�����ɁB�����H�ׂăq�g�Ɋ�������B�܂��́A������H�ׂĊ�������B�����t�ŕА߂���������āA�Z�b�c�����������śz������ƁA�L��X�������̓��ɂđ��B�A�L��X�����ǂɂȂ�B�܂��A�����ۗL�̏ꍇ�A�V���������������Ǔ��śz�����������Ɗ������N����A�S�g�ɘZ�b�c�����^��A�L�b�X�����ɂ��d�������N����B
|
�����F�������Z���t�@�������͌����@�Ō��o�B�X���ǂł͖Ɖu�f�f�@�AX��CT�ȂǁB
���ÁF���b�𒎂ɓ����B�������v���W�J���e���A���x���_�]�[���͎�ِ߂�Z���������Ɗ������N�����̂Œ��ӁB�L�b�X�����ǂ͊O�ȓI�E�o�B
�\�h�F�ؓ��̐��H�A�s���S�����������B |
���z�F���E��
�H�K���ɂ��q���Y�[���k�A�X���u�������ɑ����B
�����̓q�g�̏����㕔�ɁA�L�b�X�����͔]�A��A�牺�A���̑��S�g�̑���Ɋ���B
����𒎂��Z���i2�`3m�j�A�^�������Ȃ��A�ؓ��w�������������ł���B |
�P���
Echinococcus granulosus |
���
�������F���Ǐ�i���N���琔�\�N�j
�i�s���F�e����̕�ɂ��X��̈����Ǐ�B�̑����̎��A���t�B�x���P�A��ႁB�]���]��ᇗl�Ǐ�B |
�����j�F���ԏh��̏����ŘZ��𒎂��V�����A��Ɋ̂�t�A�B�ɓ��B���Đ����A��ƂȂ�A���̕���I�h�傪�ێ悷��ƏI�h�召���ɂ�7�T�Ő����ɂȂ�B
���ԏh��F�q�g�A�E�V�A�u�^�A�q�c�W
�I�h��F�C�k�A�L�c�l�A�I�I�J�~
�����o�H�F�I�h�傩��r�o����钎�����o���ێ�B |
�����F�E�X���j�ꂽ�Ƃ��̕���i��t���̊����\�͂̂��铪�ߌ���j�̌��o�B�y�f�R�̖@�A��̌����@�Ȃǂ̖Ɖu�w�I�f�f�@�B���h�����͋֎~�i��t�����o�ɂ����ƃA�i�t�B���L�V�[��������̂Łj�B����X���ACT�ȂǁB
���ÁF�O�ȓI�؏��i���e�t�R�o��������j���x���^�]�[���A�v���W�J���e���B
�\�h�F�I�h��A���ԏh��̌����B�H���E�H�p�b���u�̐��̋����B |
���z�F���E���B���ɖq���A�q���n�сB
�P��𒎁A����𒎂̓G�L�m�R�b�J�X�ǁi��ǁj�̕a���́B |
�����
Echinococcus multilocularis |
�P��𒎂Ɠ����o�߂����ǂ�A�̂�x�Ȃǂɕ�`���i�̕�ǁA�x��ǁj�A���炷��ɂ�ĊO���o��ɂ����͑g�D��Z�H���g�傷��B |
�����j�F���������炩�̃��[�g�Œ��ԏh��̃m�l�Y�~�A�u�^�ȂǂɐېH����A�Z�b�c���������͊̑��ŕ�ƂȂ�A�O���o��ɂ�葝��A�]�ڂ�������B���ꂪ�I�h��Ɋ����B
���ԏh��F�l�Y�~�A�q�g�A�u�^
�I�h��F�C�k�A�L�c�l
�����o�H�F�L�^�L�c�l�A�C�k�Ƃ̐ڐG�B�������ꂽ���ݐ��B�C�`�S�A�L�m�R�Ȃǂ̖쐶�A���B |
�����F��f�AX��CT�ȂǁB�P��𒎂Ɠ����B
���ÁF�P��𒎂Ɠ����B
�\�h�F�m�l�Y�~�̖o�łȂNJ����z��f���邱�ƁB |
���z�F�L�c�l�̐������鍂�ܓx�n���B�V�x���A�A�A���X�J�A�J�i�_�A���{�ȂǁB |
���^��
Vampirolepis nana |
���O�т̔j��ɂ�鉊�ǁA����ᇁB
�����A�H�~�s�U |
�����j�F���ԏh���K�v�Ƃ����A�����ŘZ�b�c�����z�����A�[�X�������環�ǂɋz���������ƂȂ�B���Ɗ������N�����B
�����o�H�F�r�o���ꂽ�����̌o���ێ�B
���ԏh��F�Ȃ��B�@�I�h��F�l�Y�~�A�܂�Ƀq�g�B |
�����F���֒��̒����̌��o�B
���ÁF���_�p�����}�C�V���A�v���W�J���e���B
�\�h�F�l�Y�~�̋쏜�A�����ɕۂB |
���z�F���E���B���ɉ��g�Ȓn��B |
�Z����
Dipylidium caninum |
��ʂɖ��Ǐ�B�Ƃ��ɐH�~�s�U�A���ɁA�����A���ӊ��B |
�������m�~�A�C�k�n�W���~�Ȃǂ��ێ�B���̑̓��őO�[�X�����A�[�X�����ƂȂ�B���̍������q�g���o���ێ悷��Ə����Ő����ƂȂ�B
�I�h��F�C�k�A�l�R |
�����F���֒��̒����̌��o�B
���ÁF�𒎏ǂ̎��ÂƓ����B
�\�h�F�C�k�A�l�R�A�����̃m�~�̋쏜�B |
���z�F���E���B�y�b�g�u�[���ɂ��l�̏Ǘ�̑����X���B�����̊����������B |
| ���NJ� |
���{�Z���z��
Schistosoma japonicum |
������:�N�����̔畆���B
�}�����F���э��ǂŒ����ǐ����������A���ǂ����Ē��Ǔ��֒E���B�S���ցA���o���B���M�A���ɁB
�������F�����������g�D�����Ċ̍d�ρ������A�x���S�B���ɔ]��Q�B |
�����j�F
���ԏh��F�{���L�B�{���L�̒��ł̓X�|���V�X�g�B�{���L�ŃZ���J���A�Y���A�q�g�Ɍo��I�Ɋ����A���s���ɖ喬�n�i�㒰�Ԗ��j�Ö��ɒ蒅���đ��B�B�����E���ɂĒ������r�o����āA�~���V�W�E�����{���L�Ɋ����B
�I�h��F�q�g�A�C�k�A�E�V�ȂǑ����̚M���ށB |
�����F�����������ړh���@�A�W���@�iAMS�V�@�j�B�Ɖu�f�f��COPT�i�����Ɣ팟�����Ƃ̊ԂɋN���钎�����͒��~�����j�B
���ÁF�v���W�J���e��
�\�h�F���s�n�ł̐��ł̐��Ƃ̐ڐG�������B |
���z�F�����A�t�B���s���ȂǃA�W�A�T�J���B���{�ł͖o�ŁB
�g�D�̒����ǐʂł͓����`�������B����𒎗����߂Ƃ����B |
�}���\���Z���z��
Schitosoma mansoni |
���{�Z���z���Ɠ��������Y���������Ȃ����ߌy�ǁB |
���ԏh��FBiomphalaria��
�I�h��F�q�g�A�`���p���W�[�ȂǑ����̚M���ށB
�����j�A�����o�H�͓��{�Z���z���Ɠ����B |
���{�Z���z���ɓ����B |
���z�F�A�t���J�A��ĂT�R�J���B
�Z���J���A�畆�������ނ̏Z���z���Z���J���A���q�g�ɐN������Ƃ��Ɍ�����畆���B |
�r���n���c�Z���z��
Schistosoma haematobium |
�A�H�Z���z���ǁ����A�B�x�̂��������ω��B�D�_�������B |
���ԏh��FBulinus��
�Z���J���A�͌o�犴�������㌌�s�����N���A��哮���p�Ȃǂɒ蒅���A�����͔A�ƂƂ��ɊO�E�֔r�o�����B |
�����F�A���ɒ����̌��o�B
��͓��{�Z���z���ɓ����B |
���z�F�A�t���J�A���ߓ��T�Q�J���B
�N�����̔����������Ȃ�B |
| �����NJ� |
�ٌ`�z��
�@�V�[�{���g�ٌ`�z��
Heterophyes heterophyes
�A�L�Q�ٌ`�z��
Heterophyes heterophyes nocens |
�S���̃J�^�������ǁ�����
�S���ٌ`�z���ǁF���������s�A�����p�s���ɐS�A�]�ȂǂɒB���A�S��S�ٖ��ɏ�Q�B |
�@��ꒆ�ԏh��F�^�e�}�L�K�C�@
��ԏh��F�{��
�A��ꒆ�ԏh��F�w�i�^���@
��ԏh��F�{���A���i�_�A�n�[�ȂǁB
�I�h��F�q�g
��ԏh��ɂă��^�Z���J���A�ɂȂ��Čo���I�Ƀq�g�̏����Ɋ����A�P�T�Ԃ��炢�Ő����ɂȂ�B |
�����F���ւŒ����̌��o�B
���ÁF�J�}���A���̌㉖�މ��܁B�v���W�J���e���B
�\�h�F�{���H���Ȃ��B |
���z�F�@�i�C���͌��n�сi�D����j�B
�A���{�A���ɐ��˓��C���݁B
���B�z�Ղ�L����B |
����z��
Metagonimus yokogawai |
�O�q�ٌ̈`�z���ǂƓ����B�����A���ɂȂǁB |
��ꒆ�ԏh��F�J���j�i
��ԏh��F�A���A���}���Ȃǂ̒W���A�D����
�I�h��F�q�g�A�C�k�A�l�R�ȂǁB��ԏh��̐��H�ɂ���Ċ����B |
�����F���ւŒ����̌��o
���ÁF�v���W�J���e��
�\�h�F�W�����̏[���ȉ��M�i���^�Z���J���A�̒�R���������j |
���z�F�A�W�A�ɍL�����z�B
���B���z�Ղ�L����B |
| �g�D�� |
�̕g
Fasciola hepatica |
���̂̊̒ʉ߂ɔ����̎����̉A�o��
�_�ǂ̕a�ςɂ��A
�}���F���t�A�̔��A���M�A�㕠���ɁA�q�f�@
�����F�_�X�ǁA�̍d�� |
�����i��������~���V�W�E���j����ꒆ�ԏh��F���m�A���K�C�i�Z���J���A�j�������A�q���i���^�Z���J���A�j���I�h��F�q�g�A�E�V�A�q�c�W�ȂǁB |
�����F���ցA�����iAMS III�@�j�D�_�������B�\��w���]���f�ɂ��_�`���e���̌���
���ÁF�v���W�J���e��
�\�h�F�����A�q���̎戵���ɒ��ӁB���ɃT���_�ɗp������^�K���V�͊������Ƃ��Ē��ӂ���B�@�@ |
���z�F���E���B���Ƀq�c�W�A�E�V�Ȃǂ̖q�{�̐���ȂƂ���B
�Q�N�ȏ����Ɣ牺�A���o�ȂǂɈُ����N���肤��B |
�̋z��
Clonorchis sinensis |
�_�ǁE�_�X���Ɋ��A�_�`��������̍d�ςƂȂ�B�����ɐH�~�s�U�A���M�A�����Ŗ��������̍d�ς������Ȃ物�t�A�n���B |
�_�ǂ��o�Ē������O�E�ց���ꒆ�ԏh��F�}���^�j�V����ԏh��F�R�C�Ȃ̊e�틛�i�ؓ����Ŕ�X���ă��^�Z���J���A�j��������I�h��F�q�g�A�C�k�A�l�R���o���I�ɐێ悵�Ċ����B |
�����F�W���@�ɂ�錟�ցB�\��w���]���f�ɂ��_�`���̒����̊m�F�B
���ÁF�v���W�J���e��
�\�h�F�W�����̔M�����B |
���z�F���{�A�����A�؍��ȂNjɓ��ɕ��z�B |
�{��x�z��
Paragonimus miyazakii |
���̂̔x�����ʂɔ����C���E�����̒����B�D�_���̑����B |
��ꒆ�ԏh��F�z���A�i�~�W���j�i
��ԏh��F�T���K�j�i�S���E���Ǔ��Ɂj
�I�h��F�C�^�`�A�C�m�V�V�A�C�k�A�e���B
�T���K�j�̐��H�ɂ���Ċ����B |
�����F�x������̒����̌��o�B�Ɖu�����w�I�f�f�B
���ÁE�\�h�̓E�F�X�e���}���x�z���Ɠ����B |
���z�F���{�e�n�B |
�E�F�X�e���}���x�z��
Paragonimus westermanii |
�����x�z���ǁF�x�����̔j��A���X��̌`���B���ǐ��������B�P��`���R���[�g�F�̌�ႁB
�]�x�z���ǁF��N�҂ɂāB�]���ւُ̈��ɂ��B�W���N�\���^�z���i�Ă�j�B
���̑��牺���Ɉُ��B |
��ꒆ�ԏh��F�J���j�i
��ԏh��F���N�Y�K�j�A�T���K�j
�������ԏh��F�C�m�V�V
���X����ɒ������Y�o����A���X����e�t�Ƌ���ႂƂ��Ě\�o�A�܂��͚�������ĕ��֒��ɔr�o�B�����ȂǂŃ~���V�W�E���A�L���ŃX�|���W�X�g�A��1,2�ヌ�W�i���o�߂��āA�Z���J���A�ƂȂ�B�L���J�j���H�ׂă��^�Z���J���A�`���B���ꂪ���̂܂܃q�g�ւ܂��̓C�m�V�V����ăq�g�o����������B
|
�����F���ւɂ��W���@�iAMS�V�@�j�BVBS���o�R���ɂ���������B
���ÁF�v���W�J���e��
�\�h�F���N�Y�K�j�A�T���K�j�A�C�m�V�V�̐��H�������B |
���z�F���A����A��A�W�A�ɍL�����z�B
�̓��ڍs�F���^�Z���J���A�������ŒE�X�����ǂ��畠�o�A���ǂɋؓ��łP�T�Ԓ���Ăѕ��o���牡�u����ʉ߁A�x�o����x�����ց����n�E�Y��
���̊Ԗ���B
���F�̐�����{�̂̂��̂ƎO�{�̂̂��̂�����B |
| �����NJ� |
��
Ascaris lumbricoides |
�c���ɂ��a�Q�F�̂̑@�ۉ��A���x���܂��̓��t���[�nj�Q�i�P�A���M�A�ċz����A�x�Z���A�D�_�������j�B
�����ɂ��a�Q�F���ɁA�H�~�s�U�A�f�C�A�_�o�ߕq�A�����ɂ�钎�����A�_���ǁB |
�c������t���̖�Ȃǂɂ��o���������㕔�����śz�������s�A�����p�s���ɔx�ց��C�njn���珬���Ő��n�i�_���Ȃǂ֖����L��j�������r�o�A�c�������
���ԏh�喳���B�I�h��q�g�B |
�����F���ցi���ړh���@�A�W���@�j�B�Y�݂̂̊ł͒����͉A���B
���ÁF�p���_�s�����e���i�R���o���g�����j�A�s�y���W���B
�\�h�F���������A�W�c���ցA�W�c�쒎�B |
���z�F�M�сE���тȂlj��g�Ŏ����Ȓn��ɑ����B
�C�k�ǁF�C�k�ɂ��c���ڍs�ǁB�̑��A��A���̑�����Ɉڍs�B���Âɂ̓`�A�x���_�]�[���B |
岒�
Enterobius vermicularis |
�����͂̂���݁i�������̎Y���̂��߁j�B�����ɐN�����������̗U���B�����ł͂���݂̂��߁A������Q�A�_�o�ߕq�ȂǁB |
��w�A�Q��A����Ȃǂɂ��o�������������ɂěz�����Ӓ��ɂĐ����ɔ��灨��Ԃ����܂ʼn����Ă��ĎY�����A���Ł�����݂̂��߂ɑ~���ނ���A�肩��Ăъ���
���ԏh�喳���A�I�h��F�q�g�B |
�����F�Z���t�@���e�[�v�ɂ����匟���@�B�i�O���A���j
���ÁF�p���_�s�����e���i�R���o���g�����j�A�A���x���_�]�[��
�\�h�F�܂���Ď�w�𐴌��ɁB�W�c�����ƏW�c�쒎�B |
���z�F���E���̊���n�≷�g�Ȓn���B�����������M�тł͂ނ��돭�Ȃ��B
�͗c�����ɑ���������B |
�Y�r�j�b��
Ancylostoma duodenale |
�b���ǁF
�畆�����t�B�����A�^�iF�^�j�c���̔畆�N���ӏ��ɐ�����B
��ؕa���Y�r�j�b����F�^�c���̌o�������ɂ��N����B�P�A�q�f�A���ɁB
�b�����n�����b���������S������z�����邽�߁B
���ɐ��������ɂ��܂̕ό`�A�ٖ��ǁB |
���ւ��璎�������u�W�`�X�^�c���iR�^�c���j�������c���ł���t�B�����A�c���iF�^�c���j���o���A�Ƃ��Ɍo��I�Ɋ����������Ő��n�A�Y���B
�I�h��F�q�g�A�u�^ |
�����F���V�@�ɂ�钎���̌��o�B
���ÁF�R���o���g����
�\�h�F����ؐ��H�̉���B�����A�W�c���ցA�쒎�B |
���z�F���[���b�p�A�A�t���J�A�A�W�A�A��ĂȂǍL�͂ɑ��݁B
��̎����L����B |
�A�����J�b��
Necator americanus |
�����c�����o�犴���B�����A�����p�ɂ̂��Ĕx�ɂđ�O���c���ƂȂ�C����`���ď����֒B���A���n���ĎY���B
�I�h��F�q�g |
���z�F���E���B
��̎���L����B |
���m�їl����
Trichostrongylus orientalis |
���������͖��Ǐ�B
���������ʼn����A���ɁA�n���i�����̏����S���h���ɂ��z���j |
�Y�r�j�b���Ɏ��Ă��ăq�g��F�^�c�����o���ێ悵�A�̓��ڍs�����ɏ����Ő��n�B
�I�h��F�q�c�W�A�E�}�A�q�g
|
�����A���ÂƂ��Ɋb���ǂƓ����B
�\�h�F���A�ʼn������ꂽ��A�Е��ɒ��ӁB |
���z�F���E���B���ɁA���ߓ��̃��N�_�A�q�c�W�Ȃǂ͍����Ɋ����B
�����͊����R�������B |
�ڒ�
Trichuris trichiura |
���������͖��Ǐ�B
���������Ŋ��ʂ̉��ǁA�������A�����A�n���B |
�c��������o���I�ɐێ恨�����śz���A���灨�Ӓ��E�������Ɋ�������O�����Ő��n�A�B |
�����F���ցi���ړh���@�A���S���a�@�j�B
���ÁF���x���_�]�[���B
�\�h�F��̐��A��w�̐����B |
���z�F���E���B���ɉ��g�Ȓn��̃q�g�Ɋ����B |
������
Strongyloides stercoralis |
F�^�c���F�x���i�x��ʉ߂��邽�߁j���t���[�nj�Q�B
�����F�����S���̃J�^�����ω��A�т��A����A���l�������B |
F�^�c�����o�犴�������s���ɔx�A�C�ǎx���o�āA�����Ɏ���A�蒅�A���n�B�Y�����āAR�^�c���������łł���B���Ɗ������邩�A���̂܂ܕ��ւɍ������ďo�āA�O�E�ɂĎ��R�������s���B
�I�h��F�q�g�A�C�k�A�l�R |
�����F���֒���R�^�c���̌��o�i���������j�B���ւ̂뎆�|�{�ɂ��F�^�c�����o�B
���ÁF�`�A�x���_�]�[��
�\�h�F���ɛ��A���܂��Ȃ��B |
���z�F�M�сE���M�т̎����Ȓn��B |
�A�j�T�L�X��
Anisakidae |
�c���ڍs��
�}������
�A�����M�[���D�����Z�����^ᇁE����� |
��ꒆ�ԏh��F�I�L�A�~
�������ԏh��F�T�o�A�X�����C�J
�I�h��F�N�W���A�C���J�������ԏh���H�ׂ邱�ƂŌo�������B |
�����F��d���e�@�B���m�N���[�i���R�̂ɂ��R�����o�@�B
���ÁF�������ɂ�钎�̓E�o�i�݁j�A�J����p�i���j�B �R���o���g����
�\�h�F�^���A�T�o�A�A�W�Ȃǂ̐��H�ɒ��ӁB |
���z�F�C�Y���H����k�C���ݏ����A���{�ȂǁB
���l�b�g�זE�i�r���@�\�j |
| ���ǁE�g�D�� |
�o���N���t�g����
Wuchereria bancrofti |
�}�����F�M����i�����p�lj����j
�������F�۔�a�A�A�X����i�����p�n�ǁA�����p�̂����A�\��E�����p�ǂ̑��B�j�B�����A�i�t�����͂̃����p�n�̕ǂɂ��A�����p�t���A���ɏo�Ă���j�B
�e���͈�ʂɖ��Q���������A�����M�[�������N�������Ƃ����遨�M�ѐ��x�D�_�������ǁi�b���l�Ǐ�j |
���ԏh��F�A�J�C�G�J�i���{�j�A�l�b�^�C�C�G�J
�I�h��F�q�g�B
���ԏh��̋z���ɂ�芴�����A�����p�n�ɊB |
�����F�w�댌�Ō��w�h���W�{�̃M���U���F�ɂċ����B
���ÁF�N�G���_�W�G�`���J���o�}�W�� |
���z�F���E�̔M�сA���M�сB
���������A�Ɠ����A�Ƌ�ʂ���ɂ́A�A�ɂP/�T�e�̃G�^�m�[���������ĐUṂ��A����ɃG�[�e���������ĐUṂ���ƌ�҂ł͓����ɂȂ�B |
�������
Onchocerca volvulus |
���̂̎��͂ɓ���g�D�`���i�I���R�Z���J��ᎁj�B�Y�o���ꂽ�e�����W�ς��Q���ȉ��̊Q�������炷�B
�畆���A��a�ρ������ɂ�����B |
���ԏh��F�u��
�I�h��F�q�g
�u���̋z���������c�����牺�ցB�牺�Ŏ�ᎌ`���B�u���͍Ăыz���̍ۂɔ牺�̎e������荞�ށB |
�����F����@�ɂ��e���̌��o�B��ᎂ�������B�}�\�b�e�B�����i�W�G�`���J���o�}�W���ɂ���ăA�����M�[�������N���邩������j�B
���ÁF�A�C�o���N�`���i�e���E���j�A�W�G�`���J���o�}�W���B��᎓E���p�B
�\�h�F�u���o�ŁB |
���z�F���A�t���J���瓌�A�t���J�A���e���A�����J |
�L���{����
Gnathostoma spinigerum |
�{�����ǁF�T�^�I�ȗc���ڍs��
�牺�g�D�ʉ߂ɔ����A�畆�̐���s�]�ƈړ����牺��ᎁB�����_�o�n��́A�x�Ȃǂɖ������B |
��ꒆ�ԏh��F�P���~�W���R
��ԏh��F���C�M���ȂǑ����̋��ށA������
�ҋ@�h��F��^�W�����A�w�r�A�l�Y�~�ȂǁB
�I�h��F�l�R�A�C�k�q�g�ւ͑�ԏh���ҋ@�h��̐��H�ɂ���Ċ������A���̂܂ܐ����ɂȂꂸ�ɑ̓��̂����������ړ�����B |
�����F�ړ����̔畆�a�ϕ��ʂ���̒��̂̌��o�i�؊J�j�B�ړ����̔畆�a�ρ{�D�_���̑����B
���ÁF���̂̓E�o�B�͊m�����Ă��炸�A��ʓI�ȃ`�A�x���_�]�[���Ȃǂ����݂��Ă���B |
���z�F�^�C�A�~�����}�[�A�����Ȃǎ�ɃA�W�A�B
�A���h�W���E�̗x��H���������{�����A�}���V�̐��H�i�{�茧�j���h�����X�{�����A���Y�h�W���E�̐��H�����{�{�����̊������N����B |
�L���Z������
Angiostrongylus cantonensis |
�c�����݂��猌�s���ɒ����_�o�����������o�ցB���͔̂]���ł͓����Ɉ͂܂�A�V�����R�[���C�f�������A�ٕ����זE��������B���̌㓪�ɁA�q�f�Ȃǂ̐����h���Ǐ�B |
���ԏh��F�A�t���J�}�C�}�C�A�i���N�W�ȂǁB
�I�h��F�l�Y�~
�����c����ۗL����i���N�W�A�}�C�}�C�̐��H�ɂ�芴������B |
�����F���t���̍D�_�������A��d�g�U�@�ȂǁB�c�ᒎ�����o����Ίm���B
���ÁF�`�A�x���_�]�[���B���ɂɑ��Ă͍��Ő��h�ɂ�鐑�t�̔r���B
�\�h�F���s�n�̒��ԏh��₱�ꂪ�G�ꂽ��ؗނ̐��H��Е��������B |
���z�F�쑾���m�̏����A�^�C�A��p�A�t�B���s���A���{�ȂǍL�����z�B
�O���㒰���点���ɓ����ł���B |
���ђ�
Trichinella spiralis |
�����i�������j�F���S���̃J�^�������ǁA�����B
�����i�}�����j�F���M�A��ʕ���A���]�B�i����ؓ��̗c���͔�X���؍זE�͔j��Ă���j
��O���i�������j�F��������A���t����S�؉���x���Ŏ��S���邱�Ƃ��B�i�c���̔�X�������j |
�����̓q�g�A�u�^�A�C�k�A�N�}�Ȃǂ̏����Ɋ��c���Y�������s�A�����p�s���ɗc��������ց����̏h�傪�ؓ��̗c����H�ׂ邱�ƂŊ����B
�q�g�ł͏b���̐��H�A����M�̃n����\�[�Z�[�W�ɂ�銴���������B |
�����F�ؐ����ɂ��c���̌��o�B��d�g�U�@�A���e�b�N�X�ÏW�����B
���ÁF���x���_�]�[���A�`�A�x���_�]�[��
�\�h�F�b���i�Ƃ��ɃN�}�A�u�^�j�̐��H�������B |
���z�F���[���b�p�A�A�����J�A�A�t���J�A����āA�^�C�B |

